Soczewki fakijne – wszystko, co musisz wiedzieć

Soczewki fakijne – wszystko, co musisz wiedzieć
Soczewki fakijne to nowoczesna alternatywa dla osób, które nie kwalifikują się do laserowej korekcji wzroku lub szukają odwracalnego rozwiązania korygującego wadę refrakcji. Dzięki implantacji soczewki między rogówkę a naturalną soczewkę oka możliwe jest skuteczne leczenie krótkowzroczności, nadwzroczności i astygmatyzmu – bez usuwania własnej soczewki pacjenta.
Zabieg ten szczególnie rekomendowany jest osobom młodym z dużą wadą wzroku, cienką rogówką lub przeciwwskazaniami do laseroterapii. W tym artykule wyjaśniam wszystkie kluczowe kwestie związane z soczewkami fakijnymi – ich zalety, wady, trwałość, rekonwalescencję oraz porównanie do zabiegu laserowego.
Soczewki fakijne – wady i zalety
Zalety:
- Nieusuwalność naturalnej soczewki – zachowana akomodacja oka.
- Odwracalność zabiegu – soczewkę można usunąć lub wymienić.
- Wysoka jakość widzenia – często lepsza niż po laserowej korekcji u osób z wysoką krótkowzrocznością.
- Bezpieczna alternatywa dla pacjentów z cienką rogówką lub nieregularnym kształtem rogówki.
- Mała inwazyjność – szybki powrót do aktywności.
Wady:
- Konieczność zachowania odpowiedniej głębokości komory przedniej oka – nie każdy się kwalifikuje.
- Ryzyko wzrostu ciśnienia śródgałkowego – może prowadzić do jaskry.
- Potencjalne przemieszczenie lub rotacja soczewki – szczególnie w przypadku modeli torycznych.
- Cena – soczewki fakijne są droższe niż laserowa korekcja, szczególnie w przypadku obu oczu.
Soczewki fakijne – skutki uboczne
Chociaż soczewki fakijne są ogólnie bezpieczne, jak każdy zabieg chirurgiczny, mogą wiązać się z powikłaniami:
- Zespół suchego oka – rzadziej niż po laserze, ale może wystąpić przejściowo.
- Zaćma – rzadko, szczególnie u pacjentów z nieprawidłową odległością między soczewkami.
- Jaskra wtórna – rzadko, spowodowana upośledzonym odpływem cieczy wodnistej.
- Endoftalmitis – ciężkie, choć rzadkie powikłanie infekcyjne.
- Halos i odblaski wokół świateł w nocy – szczególnie u osób z dużymi źrenicami.
Wybór doświadczonego chirurga okulisty oraz odpowiednia kwalifikacja minimalizują ryzyko powikłań.
Soczewki fakijne – na ile lat wystarczą?
Soczewki fakijne zaprojektowano z myślą o trwałości – nie zużywają się i nie ulegają biodegradacji. Teoretycznie mogą pozostać w oku na stałe. Jednakże:
- Średnia trwałość użytkowa to 20–30 lat, przy zachowaniu monitorowania stanu oka.
- W przypadku rozwoju zaćmy związanej z wiekiem – soczewka fakijna jest usuwana, a pacjent otrzymuje nową soczewkę wewnątrzgałkową zamiast naturalnej.
- Kontrola co 6–12 miesięcy jest kluczowa, aby ocenić klarowność soczewki i stan komory przedniej oka.
Dobrze dobrana soczewka może z powodzeniem służyć przez dekady bez potrzeby wymiany.
Soczewki fakijne – rekonwalescencja
Zabieg jest małoinwazyjny i wykonywany ambulatoryjnie – jedno oko na sesję. Typowy przebieg rekonwalescencji:
- Pierwsze 24–48 godzin – możliwe uczucie „piasku w oku”, niewielkie zamglenie.
- Kontrola po 1 dniu, 7 dniach i miesiącu – ocena położenia soczewki i ciśnienia wewnątrzgałkowego.
- Powrót do pracy – zazwyczaj możliwy po 2–3 dniach.
- Zakaz intensywnego wysiłku fizycznego, sauny, basenu – przez 2–4 tygodnie.
- Krople przeciwzapalne i antybiotykowe – stosowane przez 2–3 tygodnie zgodnie z zaleceniem lekarza.
- Dzięki precyzji zabiegu i stabilności implantów, powikłania są rzadkie, a widzenie stabilizuje się już w pierwszym tygodniu.
Podsumowanie
Soczewki fakijne to nowoczesna, bezpieczna i odwracalna metoda korekcji wad wzroku, szczególnie przydatna u pacjentów z dużą krótkowzrocznością lub przeciwwskazaniami do laseroterapii. Choć ich cena i potrzeba regularnych kontroli mogą być barierą, oferują one wyjątkową jakość widzenia i długoterminowe efekty bez ingerencji w naturalną soczewkę. Wybór między soczewkami fakijnymi a laserem powinien być dokładnie omówiony z doświadczonym okulistą – tak, by wybrać najbezpieczniejsze i najskuteczniejsze rozwiązanie dla konkretnego pacjenta.
Prof. dr hab. n. med. Iwona Grabska - Liberek
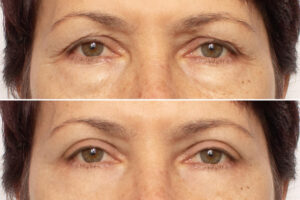
Blefaroplastyka – plastyka powiek w Libermedic
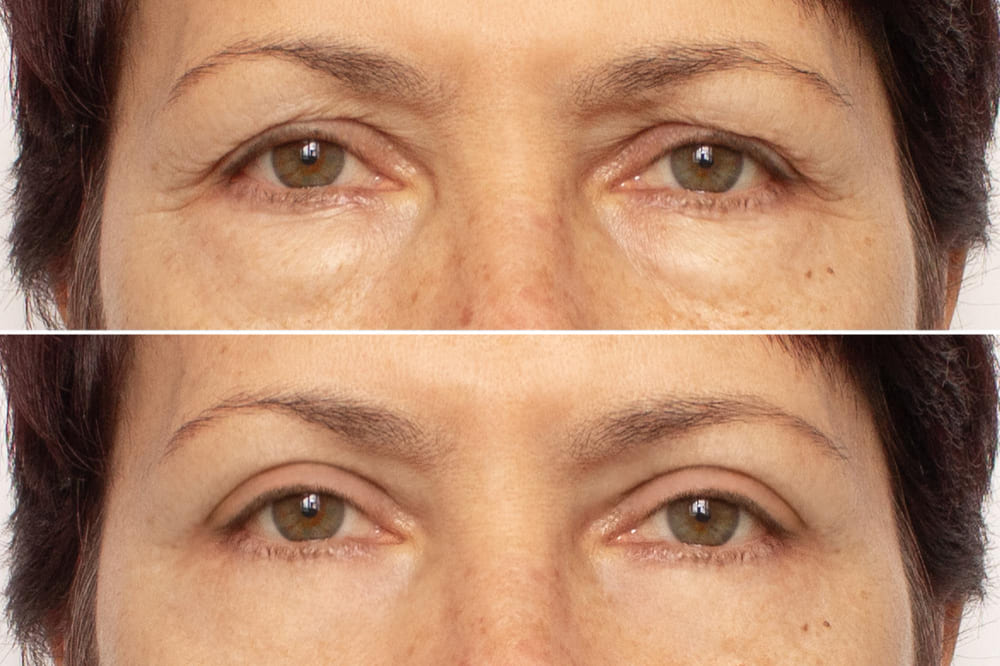
Blefaroplastyka – plastyka powiek w Libermedic
Blefaroplastyka w Libermedic – wszystko, co musisz wiedzieć: wskazania, metody, efekty, ryzyko i rekonwalescencja. Profesjonalna plastyka powiek wspierana przez zespół okuloplastyków.
Co to jest blefaroplastyka?
Blefaroplastyka (operacja powiek) to zabieg okuloplastyczny mający na celu korekcję powiek górnych, dolnych lub obu jednocześnie. Dzięki precyzyjnemu usunięciu nadmiaru skóry, tkanki tłuszczowej czy zwiotczałego mięśnia, przywraca młodszy, bardziej wypoczęty wygląd oraz poprawia pole widzenia. W Libermedic blefaroplastyką zajmują się doświadczeni specjaliści w dziedzinie Okuloplastyki, co gwarantuje bezpieczeństwo i profesjonalne podejście.
Wskazania do zabiegu blefaroplastyki
Blefaroplastyka jest rekomendowana w następujących sytuacjach:
- Zwiotczenie i nadmiar skóry powiek utrudniający widzenie lub dający efekt „drapiącego” spojrzenia.
- Worki i cienie pod oczami wynikające z przemieszczenia lub nagromadzenia tkanki tłuszczowej.
- Estetyczna potrzeba odmłodzenia wyglądu — pacjenci chcą zredukować oznaki zmęczenia i starzenia.
- Asymetria powiek bądź opadanie powiek (ptoza), które daje efekt „ciężkiego” spojrzenia.
Metody przeprowadzenia blefaroplastyki
W Libermedic stosujemy nowoczesne podejście, by każdy zabieg był indywidualnie dopasowany do pacjenta. Zabiegi okuloplastyczne wykonujemy przy użyciu nowoczesnego noża ultradźwiękowego LOKTAL który znacznie zmniejsza inwazyjność zabiegu, stopień uszkodzenia tkanek oraz skraca okres rekonwalescencji Dzięki tej technologii ryzyko powstawania blizn jest minimalne, co pozwala pacjentom cieszyć się naturalnym i estetycznym wyglądem po zabiegu. Nasze podejście zapewnia także mniejszą częstość występowania objawów niepożądanych.
Blefaroplastyka górna
- Nacięcie w naturalnej załamanej fałdzie powieki.
- Usunięcie nadmiaru skóry i częściowo tłuszczu.
- Zamknięcie cięcia cienką, niewidoczną nicią.
Blefaroplastyka dolna
- Podejście transkonjunktiwalne (bez blizn zewnętrznych) – cięcie wewnątrz powieki.
- Podejście przezskórne – wąskie cięcie pod rzęsami, usunięcie lub przeciwdziałanie opadaniu tłuszczu.
- Możliwe połączenie z liftingiem połowy twarzy dla uzyskania idealnej harmonii.
Przebieg zabiegu w Libermedic
Opis krok po kroku:
- Konsultacja wstępna/kwalifikacja do zabiegu: – przed zabiegiem każdy pacjent przechodzi szczegółowe badania w zakresie wskazań do zabiegu oraz doboru zakresu zabiegu.
- Znieczulenie – miejscowe z sedacją.
- Operacja – trwa około 1–2 godziny; dzięki precyzyjnym narzędziom i technice lekarza czas rekonwalescencji jest krótki.
- Zakładanie opatrunków – chłodzące, zmniejszające obrzęk i zaczerwienienie.
- Kontrola po zabiegu – planowana w 7 – 10 dni po zabiegu oraz 2–4 tygodnie.
Efekty blefaroplastyki – czego możesz się spodziewać
Zabieg daje:
- Ujędrnione, „otwarte” spojrzenie oraz poprawę pola widzenia – szczególnie powieki górnej.
- Redukcję obrzęków i tzw. „worków” pod oczami.
- Złagodzenie oznak starzenia – likwidacja zmarszczek i zwiotczenia.
- Trwające zwykle 5–10 lat rezultaty (czasem na stałe), przy stałym starzeniu skóry.
Rekonwalescencja – czego oczekiwać?
Typowy przebieg pooperacyjny:
- Obrzęk i zasinienie – ustępują do 10–14 dni.
- Powrót do pracy – zwykle po 7–10 dniach.
- Pełne efekty – uwidaczniają się po 4–6 tygodniach.
Dzięki doświadczeniu zespołu Libermedic czas rekonwalescencji jest możliwie najkrótszy, a pacjent szybko wraca do codzienności.
Blefaroplastyka w Libermedic – dlaczego warto?
Libermedic to klinika oferująca:
- Nowoczesne metody okuloplastyki, w tym blefaroplastyki powiek.
- Indywidualne podejście – chirurg i okuloplastyk planują zabieg dostosowany do struktury twarzy i wymagań pacjenta.
- Wysoki standard bezpieczeństwa – sterylność, monitoring i opieka pooperacyjna.
- Kompleksowa oferta – możliwość połączenia zabiegu blefaroplastyki z innymi zabiegami liftingującymi twarz.
Ponadto zabiegi okuloplastyczne w Libermedic wykonywane są przy użyciu nowoczesnego noża ultradźwiękowego LOKTAL który znacznie zmniejsza inwazyjność zabiegu, stopień uszkodzenia tkanek oraz skraca okres rekonwalescencji Dzięki tej technologii ryzyko powstawania blizn jest minimalne, co pozwala pacjentom cieszyć się naturalnym i estetycznym wyglądem po zabiegu.
Blefaroplastyka powiek – cena
Cena zależy od zakresu (powieki górne lub dolne). W celu zapoznania się z aktualnymi cenami zapraszamy na naszą podstronę Cennik.
Podsumowanie
Blefaroplastyka w Libermedic to skuteczna i bezpieczna metoda przywrócenia młodego i świeżego spojrzenia. Dzięki doświadczeniu zespołu i precyzyjnym technikom pacjenci mogą cieszyć się widocznymi efektami przy minimalnym ryzyku. Jeśli zastanawiasz się nad zabiegiem – zachęcamy do konsultacji, podczas której omówimy Twoje oczekiwania i zaplanujemy indywidualny plan działania.
Prof. dr hab. n. med. Iwona Grabska - Liberek
Czy operacja zaćmy jest bezpieczna?

Czy operacja zaćmy jest bezpieczna?
Operacja zaćmy to jeden z najczęściej wykonywanych zabiegów okulistycznych na świecie. Dzięki postępowi w technologii medycznej i doświadczeniu chirurgów, procedura ta jest obecnie uważana za bezpieczną i skuteczną metodę leczenia zaćmy. Jednak, jak każda interwencja chirurgiczna, niesie ze sobą pewne ryzyko powikłań.
Na czym polega operacja zaćmy?
Operacja zaćmy polega na usunięciu zmętniałej soczewki oka i zastąpieniu jej sztuczną soczewką wewnątrzgałkową. Najczęściej stosowaną metodą jest fakoemulsyfikacja, która wykorzystuje ultradźwięki do rozbicia zmętniałej soczewki, co umożliwia jej usunięcie przez małe nacięcie. Zabieg jest zazwyczaj przeprowadzany w znieczuleniu miejscowym i trwa około 15–30 minut.
Jakie są potencjalne powikłania?
Chociaż operacja zaćmy jest generalnie bezpieczna, mogą wystąpić pewne powikłania, takie jak:
- Zaćma wtórna: Zmętnienie torebki tylnej soczewki, które może prowadzić do pogorszenia widzenia. Zazwyczaj jest ono leczone kroplami do oczu, tabletkami, prostym zabiegiem laserowym zwanym kapsulotomią lub iniekcją doszklistkową.
- Odwarstwienie siatkówki: Rzadkie, ale poważne powikłanie, które może prowadzić do utraty wzroku, jeśli nie zostanie szybko leczone.
- Obrzęk plamki żółtej: Nagromadzenie płynu w siatkówce, co może powodować rozmycie widzenia. Zazwyczaj leczone kroplami do oczu.
- Przemieszczenie soczewki wewnątrzgałkowej: Może prowadzić do podwójnego lub nieostrego widzenia i wymagać dodatkowej interwencji chirurgicznej.
- Jaskra wtórna: Wzrost ciśnienia wewnątrzgałkowego po operacji, który może uszkodzić nerw wzrokowy, jeśli nie zostanie odpowiednio leczony.
- Zapalenie wnętrza gałki: to ciężkie i potencjalnie zagrażające wzrokowi zapalenie obejmujące wnętrze gałki ocznej — zwłaszcza ciało szkliste i/lub komorę przednią. Jest to stan nagły w okulistyce, wymagający pilnego leczenia
Warto zaznaczyć, że większość powikłań jest rzadka, a ich ryzyko można zminimalizować poprzez odpowiednie przygotowanie do zabiegu i przestrzeganie zaleceń pooperacyjnych.
Jakie są zalecenia po operacji?
Po operacji zaćmy ważne jest przestrzeganie zaleceń lekarza, które mogą obejmować:
- Stosowanie przepisanych kropli do oczu w celu zapobiegania infekcjom i stanom zapalnym.
- Unikanie ciężkiego wysiłku fizycznego i podnoszenia ciężkich przedmiotów przez kilka tygodni po zabiegu.
- Noszenie ochrony na oko podczas snu, aby zapobiec przypadkowemu urazowi.
- Regularne wizyty kontrolne u okulisty w celu monitorowania procesu gojenia.
Przestrzeganie tych zaleceń może znacznie zmniejszyć ryzyko powikłań i przyspieszyć powrót do pełnej sprawności wzrokowej.
Podsumowanie
Operacja zaćmy jest procedurą o wysokim poziomie bezpieczeństwa i skuteczności. Chociaż istnieje niewielkie ryzyko powikłań, większość pacjentów doświadcza znaczącej poprawy jakości widzenia po zabiegu. Kluczem do sukcesu jest odpowiednie przygotowanie do operacji oraz ścisłe przestrzeganie zaleceń pooperacyjnych.
Operacje zaćmy w Warszawie w klinice okulistycznej Libermedic przeprowadzane są wyłącznie przez doświadczonych chirurgów, co zdecydowanie minimalizuje ryzyko powikłań.
Jeśli zauważysz jakiekolwiek niepokojące objawy po operacji, takie jak nagłe pogorszenie widzenia, silny ból oka czy pojawienie się błysków światła, niezwłocznie skontaktuj się z lekarzem. Wczesna interwencja może zapobiec poważniejszym komplikacjom.
Prof. dr hab. n. med. Iwona Grabska - Liberek
Czego nie wolno robić po operacji zaćmy? Zalecenia

Czego nie wolno robić po operacji zaćmy? Zalecenia
Operacja zaćmy to jeden z najczęściej wykonywanych i najbezpieczniejszych zabiegów okulistycznych. Jednak sukces operacji zależy nie tylko od umiejętności chirurga, ale również od przestrzegania zaleceń pooperacyjnych przez pacjenta. Oto lista czynności, których należy unikać w okresie rekonwalescencji, aby zapewnić prawidłowe gojenie się oka i zminimalizować ryzyko powikłań.
1. Unikaj dotykania i pocierania oka
Po operacji oko jest szczególnie wrażliwe. Dotykanie, pocieranie czy drapanie może prowadzić do infekcji lub uszkodzenia gojących się tkanek. Jeśli odczuwasz swędzenie lub dyskomfort, skonsultuj się z lekarzem, zamiast próbować samodzielnie złagodzić objawy.
2. Nie narażaj oka na kontakt z wodą
Przez pierwsze dni po zabiegu unikaj mycia twarzy bezpośrednio pod bieżącą wodą. Zamiast tego, delikatnie przemywaj twarz zwilżonym ręcznikiem, omijając okolice oka. Mycie włosów powinno odbywać się z głową odchyloną do tyłu, aby woda i szampon nie dostały się do oka. Kąpiele w wannie, basenie czy naturalnych zbiornikach wodnych są przeciwwskazane przez co najmniej 4–6 tygodni po operacji.
3. Zrezygnuj z makijażu i kosmetyków w okolicach oczu
Stosowanie makijażu oczu, takich jak tusz do rzęs czy cienie, może zwiększyć ryzyko infekcji. Demakijaż wymaga pocierania, co jest niewskazane w okresie rekonwalescencji. Zaleca się unikanie makijażu przez co najmniej 4 tygodnie po zabiegu.
4. Unikaj intensywnego wysiłku fizycznego
Podnoszenie ciężarów, schylanie się czy intensywne ćwiczenia mogą zwiększyć ciśnienie wewnątrzgałkowe, co może prowadzić do powikłań. Zaleca się unikanie takich aktywności przez co najmniej 4–6 tygodni po operacji.
5. Ogranicz korzystanie z ekranów
Długotrwałe korzystanie z komputera, smartfona czy oglądanie telewizji może powodować zmęczenie oczu. W pierwszym tygodniu po operacji ogranicz czas spędzany przed ekranem do minimum.
6. Nie prowadź pojazdów bez konsultacji z lekarzem
Choć poprawa widzenia może być zauważalna już następnego dnia po operacji, pełna stabilizacja wzroku może potrwać kilka tygodni. Prowadzenie pojazdów powinno być poprzedzone konsultacją z okulistą, który oceni, czy jest to bezpieczne.
7. Unikaj podróży samolotem w pierwszym tygodniu
Zmiany ciśnienia atmosferycznego podczas lotu mogą wpływać na gojenie się oka. Zaleca się unikanie podróży lotniczych przez co najmniej tydzień po operacji, chyba że lekarz zaleci inaczej.
8. Zrezygnuj z alkoholu i kofeiny
Spożywanie alkoholu i napojów zawierających kofeinę może wpływać na ciśnienie krwi i proces gojenia. Zaleca się unikanie tych substancji przez co najmniej tydzień po operacji.
9. Nie śpij na operowanym boku
Spanie na stronie operowanego oka może wywierać nacisk na gojące się tkanki. Najbezpieczniejszą pozycją do spania jest leżenie na plecach lub na boku przeciwnym do operowanego oka. Przez pierwsze 7 -14 dni po zabiegu zaleca się noszenie specjalnej osłonki na oko podczas snu.
10. Unikaj zatłoczonych i zakurzonych miejsc
W pierwszych tygodniach po operacji unikaj miejsc, gdzie oko może być narażone na kurz, pył czy inne zanieczyszczenia. Takie środowisko zwiększa ryzyko infekcji i podrażnień.
Podsumowanie
Przestrzeganie powyższych zaleceń pomoże w szybkim i bezproblemowym powrocie do pełnej sprawności wzrokowej po operacji zaćmy. W razie wątpliwości lub niepokojących objawów, niezwłocznie skontaktuj się z lekarzem prowadzącym.
Jeśli szukasz kliniki, która przeprowadza operacje zaćmy w Warszawie, sprawdź ofertę naszego centrum okulistycznego Libermedic. Nasz zespół składa się z doświadczonych chirurgów, którzy zaopiekują się Tobą i zadbają o prawidłowy przebieg operacji.
Prof. dr hab. n. med. Iwona Grabska - Liberek
Czy laserowa korekcja wzroku jest bezpieczna?
Czy laserowa korekcja wzroku jest bezpieczna?
Laserowa korekcja wzroku od lat znajduje się w czołówce najczęściej wybieranych procedur chirurgii refrakcyjnej. Nic dziwnego – pozwala raz na zawsze pozbyć się wady wzroku i uwolnić się od okularów czy soczewek kontaktowych. Ale razem z zainteresowaniem rosną pytania. Czy laserowa korekcja wzroku jest naprawdę bezpieczna? Czy boli? Jak długo trwa taki zabieg? Pora rozwiać wszelkie wątpliwości.
Nowoczesna medycyna i bezpieczeństwo w jednym
Na wstępie warto zaznaczyć: laserowa korekcja wzroku to zabieg uznawany za jeden z najbezpieczniejszych w chirurgii okulistycznej. Został opracowany tak, by działać z ogromną precyzją, przy maksymalnym ograniczeniu ryzyka.
W renomowanych ośrodkach – takich jak centrum okulistyczne Libermedic – korzysta się wyłącznie z certyfikowanego sprzętu klasy medycznej oraz sprawdzonych technologii. Każdy pacjent przechodzi wcześniej kwalifikację – wykonujemy dokładne badania topografii rogówki, grubości, pomiar ciśnienia śródgałkowego, ocenę siatkówki i wiele innych analiz. Wszystko po to, aby nie dopuścić do operacji osób, u których występują przeciwwskazania.
Jakie metody stosujemy?
W naszym centrum okulistycznym stosujemy trzy zaawansowane technologie laserowej korekcji wzroku, które różnią się zakresem zastosowania i techniką:
EBK (Epi-Bowman Keratectomy)
Metoda powierzchowna – idealna dla pacjentów z cienką rogówką lub nieregularnym astygmatyzmem. Niezwykle precyzyjna, bezpieczna i dobrze tolerowana.
FEMTOLASIK
Połączenie lasera excimerowego Schwind Amaris z femtosekundowym laserem Zimmer. To jedno z najbardziej zaawansowanych rozwiązań dostępnych na świecie – zapewnia doskonałą jakość widzenia i wyjątkowy komfort dla pacjenta.
Presby Max Hybrid
Rozwiązanie dedykowane osobom po 40. roku życia, które chcą pozbyć się nie tylko wady do dali, ale również zależności od okularów do czytania.
Wszystkie te metody są sprawdzone klinicznie, szeroko stosowane w Europie i na świecie – a co najważniejsze – bezpieczne i skuteczne.
Czy laserowa korekcja wzroku boli?
To jedno z najczęstszych pytań, jakie słyszymy od pacjentów. I całkowicie zrozumiałe – oczy są wrażliwe, a samo słowo „laser” może budzić niepokój.
Na szczęście – nie, zabieg nie boli.
Wszystkie metody laserowej korekcji przeprowadza się w znieczuleniu miejscowym – najczęściej w postaci specjalnych kropli do oczu. Dzięki temu pacjent przez cały czas jest świadomy, ale nie odczuwa bólu.
Po zabiegu mogą pojawić się lekkie dolegliwości – uczucie „piasku pod powiekami”, łzawienie czy lekki dyskomfort przy mruganiu. Jednak to reakcje przejściowe, które ustępują najczęściej w ciągu 24–48 godzin.
Ile trwa zabieg laserowej korekcji wzroku?
To może zaskoczyć – ale sam zabieg trwa zaledwie 20-30 minut, z czego działanie samego lasera to często tylko 20–40 sekund na jedno oko. Więcej czasu zajmuje przygotowanie pacjenta i konsultacje przedoperacyjne niż właściwa procedura.
Pacjent jeszcze tego samego dnia może wrócić do domu. Po zabiegu zalecamy odpoczynek i ograniczenie ekspozycji na światło – natomiast do codziennego funkcjonowania można wrócić już po kilku dniach, zależnie od wybranej metody.
Czy zabieg może się nie udać?
Każdy zabieg medyczny niesie za sobą pewne ryzyko, ale w przypadku laserowej korekcji wzroku – ryzyko powikłań jest minimalne. Dzieje się tak dlatego, że:
- procedury są standaryzowane,
- sprzęt działa z dokładnością rzędu mikronów,
- pacjenci są wcześniej kwalifikowani do zabiegu,
- lekarze pracujący w naszym centrum mają wieloletnie doświadczenie.
Statystyki pokazują, że ponad 98% pacjentów osiąga oczekiwany rezultat bez konieczności tzw. re-touchu.
Czy to zabieg na całe życie?
Laserowa korekcja usuwa istniejącą wadę – i w większości przypadków efekt jest trwały. Jednak nie powstrzymuje naturalnych procesów starzenia oka, takich jak rozwój prezbiopii (potrzeby noszenia okularów do czytania po 40. roku życia).
Dzięki metodzie Presby Max Hybrid, oferowanej w naszym ośrodku, również ten problem można rozwiązać bezpiecznie i skutecznie.
Podsumowanie
Laserowa korekcja wzroku to bezpieczny, skuteczny i nowoczesny zabieg, który pozwala uwolnić się od wady wzroku i odzyskać komfort życia. Nie boli, trwa 20-30 minut, a jego rezultaty są długotrwałe.
Dzięki zaawansowanej technologii (EBK, FEMTOLASIK, Presby Max Hybrid) oraz zespołowi doświadczonych chirurgów, w centrum okulistycznym Libermedic wykonujemy zabiegi z najwyższą precyzją i troską o pacjenta.
Jeśli nadal masz wątpliwości – porozmawiaj z nami. Odpowiemy na każde pytanie i wspólnie zdecydujemy, czy laserowa korekcja wzroku to rozwiązanie dla Ciebie.
Prof. dr hab. n. med. Iwona Grabska - Liberek
Czy laserowa korekcja wzroku jest trwała?
Czy laserowa korekcja wzroku jest trwała?
Laserowa korekcja wzroku to jedna z najczęściej wybieranych metod eliminacji wad refrakcji, takich jak krótkowzroczność, nadwzroczność czy astygmatyzm. Pacjenci, rozważając ten zabieg, często pytają nie tylko o bezpieczeństwo czy czas rekonwalescencji, ale również o jedno z kluczowych zagadnień: czy laserowa korekcja wzroku daje trwały efekt? Odpowiedź brzmi: tak, ale pod pewnymi warunkami.
Na czym polega trwałość efektu zabiegu?
Trwałość korekcji laserowej opiera się na trwałej zmianie kształtu rogówki, dzięki której promienie światła skupiają się prawidłowo na siatkówce, co daje wyraźne widzenie. Zabieg wykonuje się raz – i w zdecydowanej większości przypadków efekt utrzymuje się przez długi czas.
Jednak ostateczny rezultat zależy od kilku istotnych czynników:
- rodzaju zastosowanej metody,
- wieku pacjenta w momencie zabiegu,
- stabilności wady wzroku przed operacją,
- ewentualnych chorób współistniejących,
- naturalnych procesów starzenia się organizmu.
Kiedy efekt jest trwały?
Zabieg laserowy nie tylko usuwa aktualną wadę, ale również poprawia jakość życia pacjenta – pozwalając na odstawienie okularów czy soczewek. U większości osób, które przeszły korekcję, ostrość wzroku pozostaje stabilna przez długi czas. To szczególnie widoczne u pacjentów, którzy:
- mieli ustabilizowaną wadę wzroku (przez minimum 12 miesięcy przed zabiegiem),
- przeszli pełną kwalifikację okulistyczną,
- nie cierpią na choroby degeneracyjne siatkówki czy rogówki,
- nie mają predyspozycji genetycznych do szybkiego pogorszenia wzroku.
Czy wada może powrócić?
W rzadkich przypadkach może dojść do tzw. regresji wady, czyli częściowego nawrotu. Dzieje się tak najczęściej u osób z dużymi wadami (np. powyżej -6.00 D) lub w wyniku naturalnych procesów, takich jak starczowzroczność (prezbiopia), która pojawia się niezależnie od przebytej korekcji laserowej – zazwyczaj po 40. roku życia.
W przypadku regresji możliwe jest wykonanie zabiegu uzupełniającego (tzw. re-touch) – pod warunkiem, że warunki anatomiczne rogówki na to pozwalają.
Różne metody zabiegów, różna precyzja
W centrum okulistycznym Libermedic, w którym przeprowadzane są zabiegi, dostępne są trzy nowoczesne metody laserowej korekcji wzroku, każda dopasowana do potrzeb pacjentów:
EBK i EBK Topoquided/Wavefrontquided
To metoda powierzchowna, odpowiednia szczególnie dla pacjentów z cieńszą rogówką lub nieregularnym astygmatyzmem. Precyzyjna modyfikacja kształtu rogówki pozwala na skorygowanie wady i utrzymanie stabilnego efektu w czasie.
FEMTOLASIK (Schwind Amaris + Zimmer Femtosekundowy)
Technologia ta zapewnia najwyższą precyzję i szybki czas rekonwalescencji. Idealna dla osób aktywnych zawodowo i sportowo. Dzięki laserowi excimerowemu i wspomagającemu femtosekundowemu, procedura jest mało inwazyjna i trwała.
Presby Max Hybrid
Innowacyjne rozwiązanie dla osób po 40. roku życia, które chcą pozbyć się zarówno wady do dali, jak i konieczności noszenia okularów do czytania. Choć starczowzroczność to proces postępujący, Presby Max Hybrid pozwala na długoletni komfort widzenia bez wspomagania okularami.
Czy efekt może się zmienić z wiekiem?
Trzeba pamiętać, że laserowa korekcja nie zatrzymuje procesu starzenia oka. Nawet jeśli zabieg usunął wadę krótkowzroczną, po 40–45 roku życia naturalnie pojawia się prezbiopia. Nie jest to jednak „nawrót wady”, tylko fizjologiczna zmiana soczewki – tak samo pojawiająca się u osób, które nigdy nie miały zabiegu.
Dla takich pacjentów dostępna jest metoda Presby Max Hybrid, która umożliwia korekcję prezbiopii w sposób komfortowy i trwały.
Podsumowanie
Czy laserowa korekcja wzroku jest trwała? – Tak, ale trwałość efektu zależy od wielu czynników, takich jak stabilność wady, metoda zabiegowa czy wiek pacjenta. Zabieg wykonuje się raz, a jego rezultaty są długoterminowe. Warto jednak pamiętać, że nasze oczy – jak każdy narząd – z wiekiem się zmieniają, dlatego niektóre procesy (jak starczowzroczność) pojawią się niezależnie od przebytej operacji.
Nowoczesne metody, takie jak EBK Topoquided, FEMTOLASIK czy Presby Max Hybrid, oferowane w naszym centrum okulistycznym Libermedic, pozwalają dobrać odpowiednią technikę do indywidualnych potrzeb – z myślą o trwałości, bezpieczeństwie i komforcie widzenia na lata.
Prof. dr hab. n. med. Iwona Grabska - Liberek
Krótkowzroczność – przyczyny, objawy i leczenie

Krótkowzroczność – przyczyny, objawy i leczenie
Krótkowzroczność, znana również jako miopia, to jedna z najczęściej występujących wad wzroku. Osoby z tą dolegliwością widzą dobrze obiekty znajdujące się blisko, ale mają trudności z dostrzeganiem przedmiotów oddalonych. Jeśli masz problem z odczytaniem numeru autobusu, rozpoznaniem twarzy z daleka lub dostrzeżeniem napisów na tablicy, możliwe, że cierpisz na krótkowzroczność. Jakie są jej przyczyny, objawy i metody leczenia? Sprawdźmy!
Czym jest krótkowzroczność?
Krótkowzroczność to wada refrakcji, w której światło wpadające do oka nie skupia się prawidłowo na siatkówce, lecz przed nią. Powoduje to niewyraźne widzenie obiektów znajdujących się w oddali. Wada ta najczęściej wynika z nadmiernej długości gałki ocznej lub zbyt dużej mocy załamywania światła przez soczewkę lub rogówkę.
Rodzaje krótkowzroczności:
- Łagodna (do -3 dioptrii) – nieznacznie utrudnia widzenie na odległość, ale można ją łatwo skorygować okularami lub soczewkami.
- Umiarkowana (-3 do -6 dioptrii) – powoduje wyraźne rozmazanie obrazu w dali, wymaga stałej korekcji.
- Wysoka (powyżej -6 dioptrii) – może prowadzić do powikłań okulistycznych, np. zwyrodnień siatkówki.
Przyczyny krótkowzroczności
- Czynniki genetyczne – jeśli jedno z rodziców jest krótkowzroczne, istnieje duże prawdopodobieństwo, że dziecko również będzie miało tę wadę wzroku. Badania wskazują, że geny mają znaczący wpływ na rozwój miopii.
- Praca wzrokowa z bliska – długotrwałe wpatrywanie się w ekrany komputerów, książki czy smartfonu powoduje nadmierne napięcie akomodacyjne, co może sprzyjać rozwojowi krótkowzroczności.
- Brak naturalnego światła – badania wykazały, że dzieci spędzające więcej czasu na świeżym powietrzu rzadziej rozwijają krótkowzroczność. Naturalne światło stymuluje prawidłowy rozwój oka i zmniejsza ryzyko postępowania wady.
- Choroby oczu – niektóre schorzenia, takie jak stożek rogówki czy cukrzyca, mogą prowadzić do rozwoju krótkowzroczności.
Objawy krótkowzroczności
- Niewyraźne widzenie w dal – rozmazane kontury obiektów znajdujących się w odległości kilku metrów.
- Bóle głowy i zmęczenie oczu – częste napięcie wzroku może prowadzić do uczucia dyskomfortu.
- Mrużenie oczu – naturalna reakcja na niewyraźne widzenie, która chwilowo poprawia ostrość obrazu.
- Problemy z widzeniem nocnym – światła uliczne i reflektory samochodów mogą wydawać się rozmazane lub powodować efekt halo.
Jeśli zauważasz u siebie te objawy, warto jak najszybciej skonsultować się z okulistą.
Jak leczyć krótkowzroczność?
Nie ma jednego sposobu leczenia krótkowzroczności, ale dostępnych jest kilka skutecznych metod korekcji:
- Okulary korekcyjne – to najprostszy i najpopularniejszy sposób na poprawę widzenia. Szkła o ujemnej wartości dioptrii pomagają prawidłowo skupić światło na siatkówce.
- Soczewki kontaktowe – szczególnie polecane osobom aktywnym fizycznie, zapewniają szerokie pole widzenia i komfort w codziennym użytkowaniu.
- Laserowa korekcja wzroku – metody takie jak FemtoLASIK i SmurtSurf, EBK, Smile pozwalają na trwałą korekcję krótkowzroczności poprzez modelowanie kształtu rogówki. Zabieg jest bezbolesny i daje szybkie efekty.
- Ortokorekcja – polega na noszeniu specjalnych soczewek kontaktowych na noc, które czasowo zmieniają kształt rogówki, pozwalając widzieć wyraźnie w ciągu dnia bez dodatkowej korekcji.
- Implanty soczewek wewnątrzgałkowych/fakijnych – stosowane w przypadkach wysokiej krótkowzroczności, gdy inne metody nie przynoszą oczekiwanych rezultatów.
Jak dbać o wzrok i zapobiegać krótkowzroczności?
- Spędzaj więcej czasu na świeżym powietrzu – minimum 2 godziny dziennie w naturalnym świetle mogą pomóc w profilaktyce krótkowzroczności.
- Dbaj o ergonomię i higienę oczu w pracy – utrzymuj ekran na odpowiedniej wysokości i odległości od oczu, stosuj regułę 20/20/20 – Co 20 minut odrywamy oczy od komputera, patrzymy na coś oddalonego od nas o co najmniej 20 stóp (około 6 metrów) przez co najmniej 20 sekund
- Regularnie badaj wzrok – kontrola u okulisty przynajmniej raz w roku pozwoli wykryć postępującą wadę na wczesnym etapie.
Podsumowanie
Krótkowzroczność to coraz częstsza wada wzroku, szczególnie wśród dzieci i młodzieży. Choć nie można jej całkowicie wyleczyć bez interwencji chirurgicznej, istnieje wiele skutecznych metod korekcji. Regularne badania wzroku i zdrowe nawyki mogą pomóc spowolnić jej postęp i poprawić komfort widzenia. Jeśli masz problem z wyraźnym widzeniem na odległość, nie zwlekaj – umów się na wizytę w naszej klinice Libermedic i zadbaj o swój wzrok!
Prof. dr hab. n. med. Iwona Grabska - Liberek
Astygmatyzm – objawy, przyczyny i leczenie

Astygmatyzm – objawy, przyczyny i leczenie
Astygmatyzm to jedyna wada wzroku, która powoduje niewyraźne widzenie zarówno z bliska, jak i z daleka. Może sprawiać trudności w codziennym funkcjonowaniu – od czytania książek po prowadzenie samochodu. Jeśli zauważasz, że kontury przedmiotów są rozmazane, linie, które powinny być proste, wydają się pochylone, a oczy szybko się męczą, warto sprawdzić, czy przyczyną nie jest właśnie astygmatyzm.
Czym jest astygmatyzm?
Astygmatyzm to wada refrakcji wynikająca z nieregularnego kształtu rogówki lub soczewki oka. Zdrowa rogówka ma kształt zbliżony do idealnej kuli, co pozwala na równomierne załamywanie światła i skupianie go w jednym punkcie na siatkówce. W oku z astygmatyzmem rogówka jest bardziej spłaszczona lub wydłużona, przypominając piłkę do rugby. Skutkuje to rozszczepieniem wiązki światła na kilka ognisk, co prowadzi do zniekształconego, nieostrego obrazu.
Wyróżniamy trzy główne typy astygmatyzmu:
- Astygmatyzm niezłożony – występuje tylko w jednej płaszczyźnie oka, w postaci krótkowzroczności lub nadwzroczności.
- Astygmatyzm złożony – w obu płaszczyznach rogówki lub soczewki występuje krótkowzroczność albo nadwzroczność ale o różnym stopniu nasilenia
- Astygmatyzm mieszany – jedno ognisko obrazu znajduje się przed siatkówką, a drugie za nią, powodując jeszcze większe zaburzenia widzenia.
Przyczyny astygmatyzmu
Astygmatyzm może mieć różne przyczyny, ale najczęściej jest to wada wrodzona, przekazywana genetycznie. Jeśli jedno z rodziców ma astygmatyzm, istnieje duże prawdopodobieństwo, że dziecko również będzie miało tę wadę wzroku.
Do innych czynników prowadzących do astygmatyzmu należą:
- Urazy oka – mechaniczne uszkodzenia mogą zmieniać kształt rogówki.
- Stożek rogówki – choroba, w której rogówka stopniowo przybiera kształt stożka, znacznie nasilając astygmatyzm.
- Blizny i zmiany pooperacyjne – niektóre operacje oczu mogą wpłynąć na strukturę rogówki.
- Nieprawidłowy rozwój oka w dzieciństwie – w niektórych przypadkach astygmatyzm pojawia się w wyniku niewłaściwego kształtowania się rogówki w trakcie wzrostu.
Objawy astygmatyzmu
Osoby z astygmatyzmem mogą doświadczać wielu uciążliwych objawów, które utrudniają codzienne funkcjonowanie. Do najczęstszych należą:
- Rozmazane widzenie – zarówno z bliska, jak i z daleka.
- Zniekształcenie obrazu – linie proste mogą wydawać się pochylone.
- Szybkie zmęczenie oczu – zwłaszcza podczas długiego czytania, pracy przy komputerze lub oglądania telewizji.
- Bóle głowy – wynikające z nadmiernego wysiłku oczu.
- Mrużenie oczu – próba poprawienia ostrości widzenia poprzez przymykanie powiek.
- Trudności z widzeniem nocnym – reflektory samochodowe i inne źródła światła mogą się rozmazywać i rozciągać.
Niektóre osoby przez długi czas nie zauważają objawów, ponieważ mózg kompensuje nieostre widzenie. Właśnie dlatego regularne badania okulistyczne są kluczowe w wykrywaniu tej wady.
Jak diagnozuje się astygmatyzm?
Jeśli podejrzewasz u siebie astygmatyzm, warto udać się do okulisty na szczegółowe badanie wzroku. Podstawowe metody diagnostyczne to:
- Badanie ostrości wzroku – test czytania liter z tablicy Snellena w różnych odległościach.
- Keratometria – pomiar krzywizny rogówki za pomocą specjalistycznego urządzenia.
- Topografia/tomografia rogówki – komputerowe skanowanie przedniej i tylnejpowierzchni rogówki, które pozwala wykryć nawet niewielkie nieregularności.
- Refraktometria – komputerowe badanie refrakcji oka, określające stopień i rodzaj wady wzroku.
Jak leczyć astygmatyzm?
Nie ma jednej metody leczenia astygmatyzmu, ale istnieją skuteczne sposoby jego korekcji. Wybór odpowiedniego rozwiązania zależy od stopnia zaawansowania wady i preferencji pacjenta.
- Okulary korekcyjne – wyposażone w soczewki cylindryczne, które kompensują nierównomierne załamywanie światła.
- Szkła kontaktowe toryczne – dostosowane do kształtu rogówki, zapewniające szersze pole widzenia niż okulary.
- Laserowa korekcja wzroku – metoda trwałego usunięcia astygmatyzmu poprzez modelowanie rogówki za pomocą lasera.
- Soczewki fakijne – doszczepiane do oka ,stosowane w przypadkach, gdy laserowa korekcja nie jest możliwa.
Jak dbać o wzrok przy astygmatyzmie?
- Po pierwsze dobór okularów lub soczewek kontaktowych korekcyjnych
- Dbaj o odpowiednie oświetlenie – unikaj pracy w półmroku, ponieważ może to dodatkowo męczyć oczy.
- Regularnie badaj wzrok – co najmniej raz w roku odwiedzaj okulistę, by monitorować postęp wady ( dotyczy to każdej wady wzroku)
- Unikaj długiego wpatrywania się w ekrany – ogranicz czas spędzany przed komputerem i telefonem.
Podsumowanie
Astygmatyzm to wada wzroku, która może znacząco wpłynąć na komfort codziennego życia. Na szczęście nowoczesna okulistyka oferuje skuteczne metody diagnostyki i korekcji tej wady. Jeśli zauważasz u siebie objawy, warto jak najszybciej skonsultować się z naszą kliniką Libermedic, aby dobrać najlepszą metodę korekcji i uniknąć dalszych problemów ze wzrokiem. Pamiętaj, że zdrowe oczy to lepsza jakość życia!